Reações químicas são fantásticas. Substâncias se transformando em outras, com propriedades totalmente diferentes. Bolhas de gás podem aparecer quando misturamos dois líquidos. Cores podem mudar ao cair de uma gota sobre um frasco cheio de líquido. Um sólido pode aparecer, tornando o líquido opaco. Todos grandes exemplos de pistas de que uma reação química aconteceu quando misturamos soluções. Mas eu creio que nenhuma dessas evidências de reação química é tão misteriosa ou espetacular quanto o que acontece quando uma reação química libera luz.
Fazer uma reação química que libera luz, a luz “fria” que é liberada em um processo quimioluminescente costumava ser algo bem complicado, uma vez que em geral são necessários reagentes bem específicos e de difícil acesso. Isso mudou com o aparecimento das “pulseiras de luz”, que trazem a reação ao alcance de qualquer situação, seja pelo baixo custo como pela maneira segura em que a reação é conduzida.
Usando na sua aula
Você pode demonstrar a liberação de luz pela pulseira simplesmente entortando e quebrando o tubo de vidro no interior da pulseira. Se for possível, apagar as luzes da sala pode ajudar na visualização, mas em geral a luz da pulseira é brilhante o suficiente para ser vista mesmo em uma sala iluminada.
Vamos usar a pulseira de luz para mostrar alguns dos fatores que influenciam na velocidade de uma reação química, como a temperatura e presença de um catalisador.
Efeito da temperatura
Para demonstrar o efeito da temperatura na emissão de luz, você vai precisar de dois recipientes altos e de água quente e gelada. Coloque água quente em um dos recipientes e água gelada no outro. Inicie duas pulseiras de luz de mesma cor ao mesmo tempo. Insira uma pulseira na água quente e outra na água gelada. Observe o que acontece após alguns segundos. Retire as pulseiras e coloque a que estava na água quente na água fria e vice-versa. Observe mais alguns segundos. O vídeo abaixo mostra o que acontece.


Catalisador
Uma outra maneira de se alterar a velocidade de uma reação química envolve a adição de um catalisador. Um catalisador é uma substância que possibilita um caminho alternativo e mais rápido para a reação. Esse caminho alternativo envolve uma reação do catalisador com um dos reagentes, formando um ou mais passos intermediários e que no final restauram o catalisador, permitindo que ele consiga reagir novamente, formando um ciclo.
Para observarmos o efeito de um catalisador na reação da pulseira de luz, vamos precisar abrir a pulseira e separar seus componentes. Você pode usar uma tesoura comum e cortar uma das pontas do tubo (tomando cuidado para não quebrar o tubo de vidro. Vire o lado cortado do tubo para baixo, inserindo-o em um frasco. Corte a outra ponta e recolha todo o líquido. Retire o tubo de vidro e limpe-o bem. Usando um óculos de proteção e envolvendo o tubo de vidro com um pano, quebre uma das suas pontas (você pode usar um alicate de corte para isso). Insira a ponta quebrada em outro frasco e quebre a outra ponta do tubo de vidro, recolhendo o líquido.
Agora que temos os reagentes podemos observar a reação colocando algumas gotas de cada reagente em uma pasta plástica. Após observar a luz emitida, adicione uma pequena quantidade de salicilato de sódio e misture bem. O aumento da emissão de luz é muito visível.
Podemos usar outras substâncias como catalisadores, como por exemplo o carbonato de sódio. O catalisador deve ser uma substância com caráter básico. Veja no vídeo abaixo como o catalisador faz com que muito mais luz seja emitida em um curto espaço de tempo, consumindo rapidamente os reagentes.
O que acontece
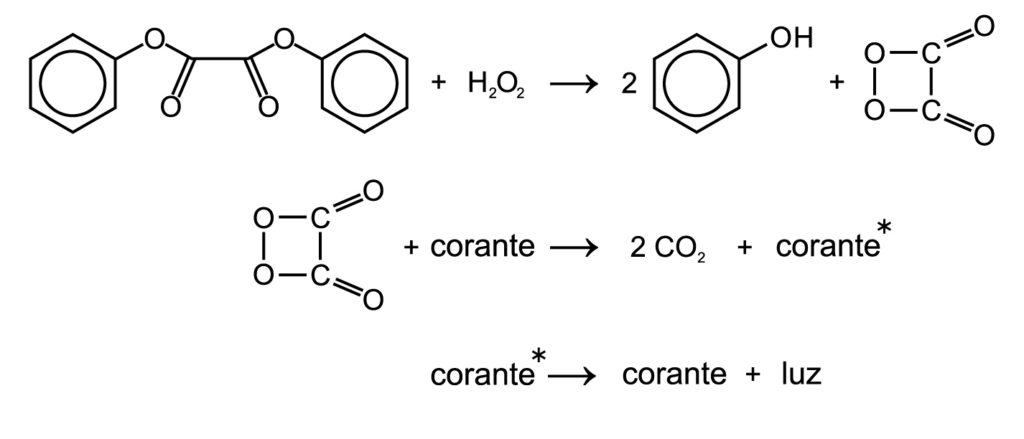
Essa espécie reativa transfere energia para o corante fluorescente ao se quebrar, formando duas moléculas de gás carbônico. O corante fluorescente vai para um estado de maior energia (estado excitado, representado pelo *). O corante então retorna ao seu estado de menor energia, liberando luz. Com este sistema, basta mudar a molécula do corante e podemos ter pulseiras que emitem cores diferentes.
Além disso, podemos ver que o processo todo consome os reagentes, e quando os reagentes forem gastos, a reação acaba e não temos mais emissão de luz. Podemos aumentar ou reduzir a velocidade da reação, emitindo mais ou menos luz por segundo, mas a quantidade total de luz que será produzida pela pulseira depende apenas da quantidade de reagente presente.
Se você quiser saber mais sobre as pulseiras e a catálise, veja o vídeo que gravei com o Manual do Mundo abaixo.
Finalmentes
As pulseiras de luz podem ser usadas para explorar alguns dos fatores que afetam a velocidade de uma reação química de maneira simples, visual e com baixo custo.
Gostou dessa ideia? Compartilhe com seus colegas e deixe um comentário abaixo.

